Лекция 4 - Образование оксидной пленки на поверхности металла
План лекции:
1. Образование оксидной пленки
2. Защитные свойства оксидных пленок
1. Образование оксидной пленки
Даже при комнатной температуре на поверхности многих металлов на воздухе образуется тончайший слой оксидов.
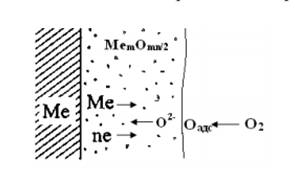
Схема образования оксидной пленки на металле
Образование продуктов коррозии осуществляется в результате протекания ряда последовательных и параллельных реакций
1.ионизация металла и переход его в форме ионов и электронов в слой оксида;
2.перемещение ионов металла Меn+ и электронов в слое оксида;
3.перенос кислорода из газового потока к поверхности оксида;
4.адсорбция кислорода на поверхности;
5.превращение адсорбированного кислорода в ион О2– ;
6.перемещение ионов кислорода О2– в слое оксида;
7.реакция образования оксида.
В результате такого взаимодействия образуется сначала мономолекулярный, а затем полимолекулярный слой оксидов. В дальнейшем атомы кислорода диффундируют через образовавшийся слой оксида, одновременно с этим в противоположном направлении диффундируют ионы металла. Реагируя с кислородом, ионы металла образуют оксид. Это приводит к появлению новых слоев пленки, т. е. к ее утолщению.
При нагреве растет толщина оксида и изменяется его кристаллическая структура: решетка оксида, по мере удаления от поверхности металла все больше приближается к решетке компактного оксида.
По мере утолщения пленки процесс диффузии будет затрудняться. Возникающая пленка будет тормозить дальнейшее развитие коррозионного процесса только в том случае, когда она будет обладать защитными свойствами. В связи с этим важно знать свойства образующихся пленок, механизм и законы их роста, отношение пленок к влиянию различных внешних факторов (температуре, рН среды, давлению и др.). Так, например, защитные свойства толстых оксидных пленок, образующихся при высоких температурах, определяются способностью оксидного слоя целиком покрывать поверхность металла и проницаемостью самого оксида для ионов металла и кислорода. Кроме этого, толщина образовавшихся пленок обусловливается видом металла, параметрами среды и рядом других факторов.
2. Защитные свойства оксидных пленок
Образовавшаяся оксидная пленка может защищать металл от дальнейшего окисления. Толщина пленок, образующихся при взаимодействии металлов с сухим воздухом или другими окислителями, зависит от природы металла, характера среды, температуры и других факторов. По толщине пленки можно разделить на следующие три группы:
1) тонкие, невидимые (толщина менее 40 нм);
2) средней толщины, дающие цвета побежалости (толщина 40-500 нм);
3) толстые, видимые (толщина более 500 нм).
Чтобы оксидная пленка обладала защитными свойствами, она должна удовлетворять следующим требованиям:
– быть сплошной, беспористой;
– иметь хорошее сцепление с металлом;
– иметь коэффициент термического расширения, близкий к величине этой характеристики для металла;
– быть химически инертной по отношению к данной агрессивной среде;
– обладать твердостью и износостойкостью.
Если образовавшаяся оксидная пленка пористая, рыхлая и обладает плохим сцеплением с металлом, то даже при условии ее инертности к данной агрессивной среде она не будет защитной.
Основным условием предотвращения дальнейшего окисления металла, покрытого оксидной пленкой, является беспористость этой пленки, ее сплошность. Возможность образования такой сплошной пленки определяется соотношением объемов образованного оксида и окисленного металла. Условие сплошности пленок было сформулировано Пиллингом и Бедворсом и заключается в следующем.
Если объем химического соединения (например, оксида Vок) меньше, чем объем металла (VМе), образующего это соединение, можно ожидать получения несплошной, пористой пленки, обладающей слабыми защитными свойствами. При обратном соотношении Vок и VМе можно ожидать образования сплошных пленок, способных защищать металл от коррозии. Объем металла равен:
VMe = A/d,
где А – атомная масса металла;
d – плотность металла.
Объем полученного оксида будет равен:
Vok = ![]() ,
,
где М – молекулярная масса оксида;
n – число атомов металла в молекуле оксида;
D– плотность оксида.
То есть, если
![]() =
= ![]() < 1
< 1
пленка не будет сплошной, а если ![]() > 1, пленка может быть сплошной.
Значения этой величины рассчитаны для металлов. Например, металлами, имеющими
> 1, пленка может быть сплошной.
Значения этой величины рассчитаны для металлов. Например, металлами, имеющими ![]() < 1 являются – К,
Na, Ca, Ba, Mg, которые образуют рыхлые пленки со слабыми защитными свойствами.
Величину
< 1 являются – К,
Na, Ca, Ba, Mg, которые образуют рыхлые пленки со слабыми защитными свойствами.
Величину ![]() > 1 имеют многие металлы, например
Al, Sn, Ti, Zn, Ni, Cr, Fe и др. Их оксидные пленки тормозят дальнейшее
окисление металла. Однако в ряде случаев могут быть отклонения от этой
закономерности. Например, в реальных условиях в пленке в процессе ее роста могут
возникать напряжения, разрушающие пленку. Может иметь место также недостаточная
пластичность пленки, летучесть оксидов и т.д. В зависимости от природы металла
рост пленок подчиняется различным закономерностям. Например, в реальных
условиях в пленке в процессе ее роста могут возникать напряжения, разрушающие
пленку. Может иметь место также недостаточная пластичность пленки, летучесть
оксидов и т.д. Vок / VМе>1
> 1 имеют многие металлы, например
Al, Sn, Ti, Zn, Ni, Cr, Fe и др. Их оксидные пленки тормозят дальнейшее
окисление металла. Однако в ряде случаев могут быть отклонения от этой
закономерности. Например, в реальных условиях в пленке в процессе ее роста могут
возникать напряжения, разрушающие пленку. Может иметь место также недостаточная
пластичность пленки, летучесть оксидов и т.д. В зависимости от природы металла
рост пленок подчиняется различным закономерностям. Например, в реальных
условиях в пленке в процессе ее роста могут возникать напряжения, разрушающие
пленку. Может иметь место также недостаточная пластичность пленки, летучесть
оксидов и т.д. Vок / VМе>1
В зависимости от природы металла рост пленок подчиняется различным закономерностям (рисунок).
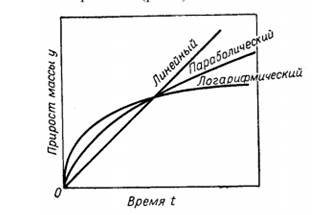
Рисунок - Графики, иллюстрирующие законы окисления металлов
Для металлов, имеющих соотношение ![]() < 1 (щелочных и
щелочноземельных), когда пленки не обладают защитными свойствами, толщина
пленок подчиняется линейному закону роста:
< 1 (щелочных и
щелочноземельных), когда пленки не обладают защитными свойствами, толщина
пленок подчиняется линейному закону роста:
y = Kτ,
где y – толщина пленок;
τ– время окисления;
К – постоянная.
Если пленка обладает защитными свойствами, то по мере ее роста скорость окисления уменьшается. Чем более высокими защитными свойствами обладает пленка, тем меньше скорость диффузии окислителя через нее и меньше скорость ее роста. Возможна параболическая зависимость:
y2 = Kτ .
В некоторых случаях рост пленок идет с сильным затуханием по логарифмической зависимости:
y = ln(kτ).
Пленки, растущие по этому закону, обладают лучшими защитными свойствами, например, для меди, никеля и железа в соответствующем интервале температур.
Условием, или критерием, сплошности, позволяющим оценить возможность образования на металле сплошной оксидной плёнки, может служить отношение молярного объема оксида к объему металла, пошедшего на его образование. Для образования сплошной пленки это отношение должно находиться в пределах:
1<![]() < 2.5
< 2.5
где ![]() , – молярные
объемы оксида и металла, соответственно;
, – молярные
объемы оксида и металла, соответственно;
Если указанное отношение меньше единицы, то образующегося объема оксида не хватает для того, чтобы полностью покрыть поверхность металла, оксидная пленка получается пористой. При достаточно большой величине данного отношения (≥2,5) в образующейся пленке возникают большие внутренние напряжения, которые приводят к ее разрушению.